多形胶质母细胞瘤(GBM)是一种极其致命的脑癌,是一种严重的黑盒挑战。要观察这些肿瘤在自然环境中是如何运作的几乎是不可能的,而动物模型并不总是能提供好的答案。
但是现在,索尔克研究所的研究人员朝着迎接这一挑战迈出了重要的一步。索尔克的科学家们只在人类大脑类器官的几个细胞中编辑了两个基因,就产生了侵略性的GBM肿瘤。这种新模型可以用于研究肿瘤进展,研究新药,甚至为患者提供个性化治疗。这项研究于2018年4月24日发表在《细胞报告》杂志上。
困扰临床试验的一个问题是,通常在动物身上有效的药物在人身上不起作用。研究人员试图通过异种移植来克服这一问题,在异种移植中,患者的肿瘤组织被植入动物模型中,但这种方法有其自身的问题。有时,没有足够的人类肿瘤组织来研究,随着时间的推移,肿瘤会适应它们的新家。
Salk高级研究员、论文第一作者小川纯子(Junko Ogawa)表示:“随着肿瘤在小鼠体内生长,环境会改变肿瘤的特征。”“我们不知道它是否与患者最初的癌症相似。”
解决方案可能是人类大脑的类器官,其中包含神经元和其他脑细胞。索尔克实验室已经使用干细胞在培养皿中生成这些小的(约4毫米)3D结构有一段时间了,他们想研究如何将其应用于GBM的研究。
他们使用CRISPR-Cas9工具在一个类器官的几个细胞中编辑了两个与癌症密切相关的基因,HRas和p53。HRas是一种癌症致癌基因,可以促进细胞的快速生长,而p53是一种肿瘤抑制因子。换句话说,他们松开刹车,踩油门。
这些类有机物在培养皿中变成了肿瘤样结构,它们生长迅速,并有几个与GBM相关的生物标志物。最终,他们接管了类器官,用肿瘤组织取代了原来的细胞。此外,它们还可以被连续移植到动物模型中,在动物模型中它们的攻击性也很强。
这种方法有许多优点。仅仅在几个细胞中编辑p53和HRas就能更好地复制GBMs在人体内的发育过程——它们不是像异种移植那样一次产生数千个细胞,而是一两个异常细胞。
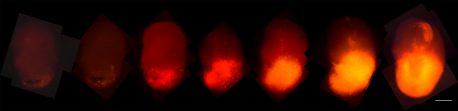
研究小组在致癌的HRas中添加了一种名为tdTomato的荧光红色标记物。当这些细胞接管类有机物时,研究人员可以追踪它们的进展。此外,当这些类器官肿瘤被移植到小鼠大脑中时,它们生长迅速,与取自患者的肿瘤相似,因此更容易获得样本。
小川说:“你可以在老鼠身上观察肿瘤的特性,现在我们可以给它们用药,看看是否有效。”我们还可以测试肿瘤侵袭正常脑组织的能力。
这些类有机物还可以作为人体肿瘤样本和一些GBM细胞系的宿主。该模型可用于个性化护理。研究人员和临床医生可以从病人身上移植癌细胞来制作器官模型。因此,他们可以研究肿瘤在匹配患者基因组的细胞中对治疗的反应。虽然类器官缺乏内皮细胞和免疫系统(这将使它们更加复杂,并帮助它们更好地复制实际的脑组织),但这个模型可能在研究各种脑转移癌方面非常有用,而不仅仅是GBM。



